尽管最近努力增加全基因组关联研究(GWASs)的多样性,但由于可用的GWASs中潜在的样本选择偏差,目前与肾功能相关的大多数位点仍然局限于欧洲血统。我们在80027名来自英国生物银行(UKBB)、百万退伍军人计划(MVP)和慢性肾脏疾病遗传(CKDGen)联盟的非洲裔个体中确定与估计肾小球滤过率(eGFRcrea)相关的易感位点。
我们确定了8个先导snp,其中7个先前与其他人群的eGFR相关。我们发现了一个新的变异,rs77408001,这是一个映射到ELN基因的内含子变异。我们验证了三个先前报道的ggatm - spata5l1、SLC15A5和AGPAT3位点。精细映射分析发现变异rs77121243和rs201602445有99.9%的后验概率是因果关系。我们的研究结果保证了在非洲血统的个体中设计更大的研究,以获得对慢性肾脏疾病(CKD)发病机制的新见解,并确定可能影响肾功能和疾病的非洲血统特有的基因组变异。
慢性肾病(Chronic kidney disease, CKD)被定义为肾脏损害或肾小球滤过率(glomerular filtration rate, eGFR)≥60ml /min/1.73m2持续3个月以上[1]。全球成人CKD患病率估计约为10%[2],撒哈拉以南非洲地区的患病率估计为13.1%[3]。CKD的护理和管理对全球医疗保健系统造成了重大的财政负担,在发展中经济体,尤其是在非洲[4]。
与CKD相关的遗传风险因素是由种族驱动的,包括但不限于端粒长度、拷贝数变异(CNVs)和线粒体DNA[5]。许多与肾小球滤过率(eGFR)相关的基因座主要是通过欧洲和亚洲血统的全基因组关联研究(GWAS)发现的[6,7,8]。eGFR是确定CKD的肾功能指标。由于全球GWASs的系统性样本选择偏差,许多在欧洲中心人群中发现的重要基因座很难在非洲祖先群体中复制。这归因于不同祖先间连锁不平衡(LD)、遗传力和等位基因频率的差异[5,9,10,11,12]。据报道,两个关键基因的多态性,即血浆激肽肽基因(KLKB1)和啮齿动物肾衰竭基因的人类同源基因,与美国黑人人群中终末期肾病(ESRD)的相关性高于白人[13]。
在过去的15年里,通过增加以前未被充分代表的祖先(如非洲祖先)的数量,人们努力增加对复杂性状进行GWASs的队列的多样性[14,15,16,17]。然而,这些努力仍然受到各种后勤挑战的限制。因此,在大多数全球财团中,由于潜在的对欧洲血统个体的抽样偏差而导致的低功率仍然是突出的[18,19]。大多数此类研究都将非洲裔人口作为跨种族分析的小型验证队列,主要是为了与更大的欧洲裔队列进行比较。这并没有产生太多的CKD特异性基因位点的发现。因此,这样的研究设计可能会错过这些全球联盟中非洲血统个体特有的一些基因座。
因此,我们的研究利用了eGFRcrea GWAS的汇总数据,这些数据仅来自三个全球联盟:百万退伍军人计划(MVP)、英国生物银行(UKBB)和慢性肾脏疾病遗传联盟(CKDGen),总样本量超过8万名非洲血统参与者。我们旨在揭示这些个体中与CKD相关的基因座,通过全表型关联分析进一步表征其功能和表型关联,并使用贝叶斯精细映射方法确定变异的因果关系。
对来自两个全球人群联盟:UKBB[20]和CKDGen[21]以及一个基于医院的队列,MVP[22]的80,027名非洲血统个体的eGFR的GWAS汇总统计数据进行meta分析。研究样本特征总结如表1所示。参与本研究的队列的更多细节见方法部分和补充材料。
表1研究队列的特征
我们分析了22.6万个SNPs和403个SNPs获得全基因组显著性(P < 5 X 10E-8)。我们通过在显著snp周围±500 kb窗口聚集鉴定出先导snp,并鉴定出8个先导变异。其中7例与eGFRcrea有关。meta分析中最小且最全基因组显著的p值为1.326e-38,标记为15:45592887。图1总结了三个队列的非洲血统eGFRcrea荟萃分析结果。我们的功率计算表明,在我们的分析中,确定全基因组意义的功率为80%。
图1
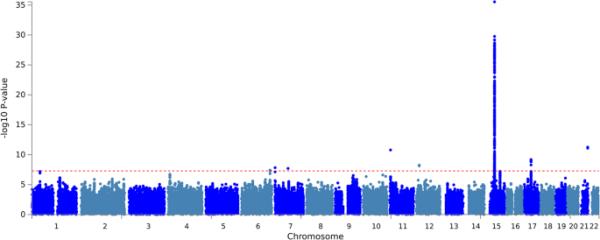
meta分析结果的曼哈顿图显示-log10 (P值)与eGFRcrea的基因组位置图相比。已知的铅变体用红色表示,新的铅变体用绿色表示
SNP rs201602445位于第15染色体上,碱基位置45592887,相关性最强(p值=1.326e-38,图1,Supplementary Table s1)。该SNP位于ggatm -SPATA5L1位点的精子发生相关5-like 1 (SPATA5L1)附近。我们发现了一个内含子变异rs77408001,映射到ELN基因(表2,图2),以前没有与eGFRcrea相关,因此我们认为这是一个新的SNP。该SNP在乌干达基因组资源(UGR)数据集中通过代理复制[25]。代理SNP为rs141339897 (chr7:73727705)(在MSL单体型中r=1, D '=1),如表2所示。其他被代理复制的SNP见补充表s6,最显著的被代理SNP (rs3135654)的位点放大图见补充图s3。
表2全基因组显著位点(P< 5 × 108)与eGFR相关ta-analysis
图2
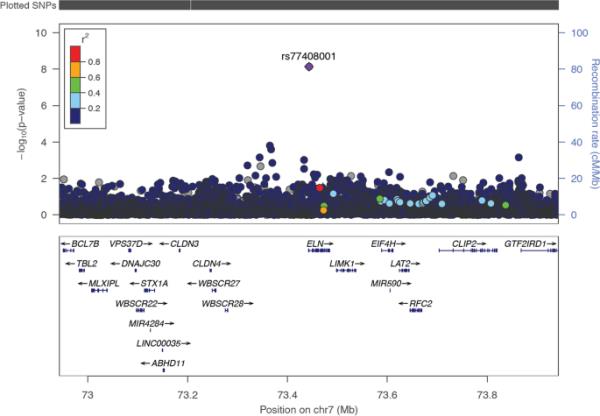
在ELN位点,来自UKBB和MVP联盟的> 80k非洲血统个体的eGFR区域关联图。先导SNP rs77408001呈紫色。使用来自1000个基因组的非洲血统参考面板计算该位点与其他snp的LD (r2)。箭头表示转录方向
铅SNP rs10084572位于21号染色体上的1-酰基甘油-3-磷酸o -酰基转移酶3 (AGPAT3)附近,而铅SNP rs200950799位于12号染色体上的溶质载体家族15,成员5基因(SLC15A5)附近,先前报道与非西班牙裔黑人的eGFRcrea相关。关于主要snp遗传结构的进一步信息用补充图s1中的区域关联图来说明。
我们对meta分析结果进行了基因组控制校正,以解释通货膨胀。我们没有发现任何证据表明,由于剩余种群结构,每个队列中个体之间的预期等位基因频率存在显著差异,如图3所示。膨胀λ为1.07,表明测试统计中的偏差最小。
图3
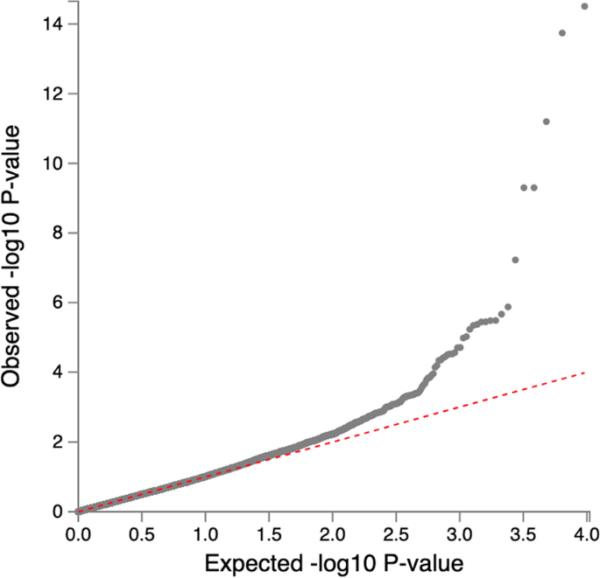
基于血清肌酐的eGFR全基因组关联的分位数图
基于meta分析中每个主要snp的±500 kb窗口进行贝叶斯精细映射。两个变异,rs77121243和rs201602445,每一个都有一个可信集,占99%的后验概率(PP)驱动非洲血统个体的eGFR关联。SNPs 12:17157119和21:45412872,每个可信集大小为2,占因果SNPs PP的99%。变体7:73443012 (rs77408001)、12:17157119 (rs200950799)和21:45412872 (rs10084572)的可信集大小分别为5、2和2(补充表s2)。然后,我们继续比较这些基因座在EUR GWAS中的99%可信集大小。与EUR GWAS相比,它们在AFR中的99%可信集大小较小,但7:1286192个位点除外(补充表s3)。这表明AFR GWAS比EUR GWAS提高了精细制图分辨率。
我们对基因型组织表达(GTEx)、NephQTL[26]、人类肾脏eQTL图谱[27]和RegulomeDB[28]进行了肾脏表达数量性状位点(eQTL)分析。我们在GTEx数据库中发现了3/8先导snp的显著等位基因;rs9908131、rs10945657和rs13230509(补充表5),P < 5E-8)。变异:rs9908131和rs10945657在GTEx和NephQTL资源中都有显著的对等qtl。变异rs13230509与NephQTLs中的任何eqtl均无显著相关性。对于三个具有显著eqtl的变异,我们得出结论,eGFR关联和eqtl之间存在共定位的证据。所有8个先导snp在人类肾脏图谱中都不是显著的等位基因。所有显示显著eqtl的先导snp都被定位到非肾脏组织。使用RegulomeDB,我们没有发现任何证据表明先导snp和任何高LD的snp对调节有影响。
在所有的先导snp中,有7个与其他表型显著相关。显示最显著关联的SNP变异及其表型见补充表4。变异rs77121243和rs13230509分别与代谢和血液学性状相关最显著。我们进一步进行了MAGMA组织表达分析,但没有一个变体在肾脏中有显著表达。
摘要
介绍
结果
讨论
方法
数据和材料的可用性
参考文献
致谢
作者信息
道德声明
补充信息
搜索
导航
#####
我们提出了基于血清肌酐的非洲血统个体eGFR的GWAS汇总统计数据的荟萃分析结果。据我们所知,这是为数不多的结合3个主要全球GWAS联盟(UKBB, CKDGen和MVP)中严格非洲血统个体eGFRcrea汇总统计的研究之一。
在我们的分析中发现的主要snp中,没有一个先前在欧洲祖先中被报道与eGFRcrea相关。我们验证了七个变异,这些变异与先前报道的非洲血统个体的eGFR位点相对应;GATM/SPATA5L1, SLC15A5,和AGPAT3[7,8]。关联最显著的首个SNP位于GATM/SPATA5L1位点附近,之前被定位为非洲大陆其他地方的肌酐合成[25]。这一先导SNP不同于欧洲血统个体中类似定位到GATM位点的SNP[6,24]。GATM是一种通过编码甘氨酸氨基转移酶参与肌酐生物合成的酶。据报道,GATM位点的snp对血清肌酐水平有影响,但不影响欧洲血统个体对肾脏疾病的易感性[7,24]。最近在非洲大陆也有类似的报道[25]。变异rs13230509先前在非西班牙裔黑人和非西班牙裔白人中与eGFRcrea相关[24]。
基因座SPATA5L1是已知的eGFR基因座[6]。此前有报道称该基因座与欧洲血统个体的eGFR相关[8]。SPATA5L1编码蛋白的作用机制影响肾脏功能,其在肾脏组织中的丰富程度尚不清楚。同样,SLC15A5先前也与欧洲人的eGFR有关[24]。SLC15A5编码一种能激活同体转运蛋白的蛋白质。它是膜的一个组成部分,预计参与多肽运输,蛋白质运输和跨膜运输。
其中一个先导SNP rs77408001位于ELN基因中,尚未被定位到任何eGFR位点。这种基因编码一种蛋白质,是两种弹性纤维成分之一。ELN基因,也被称为弹性蛋白基因,编码一种叫做对流层弹性蛋白的蛋白质,弹力蛋白就是由这种蛋白质合成的。弹性蛋白是支撑人体结缔组织的弹性纤维的主要成分[29]。该基因7q11.23的缺失突变与Williams综合征(WS)有关,WS以心血管疾病为特征,包括弹性蛋白动脉病变、外周肺狭窄、瓣上主动脉狭窄和高血压[30]。
贝叶斯精细映射分析确定了两个领先的snp, rs77121243和rs201602445,单个可信集大小分别显示出99.9%的后验概率在各自的位点驱动关联。先导SNP;Rs201602445,位于特征位点附近;在非洲裔人群中,GATM与血清肌酐显著相关[25]。总体而言,与欧洲GWAS相比,非洲血统GWAS的聚合提高了精细制图分辨率。
大多数先导变异在公开的肾脏基因表达资源中不具有显著的数量性状位点(quantitative trait loci, eQTLs)表达,且不共定位于任何肾脏组织。考虑到这些资源在人群中缺乏普遍性,这不足为奇。例如,超过80%的数量性状位点(quantitative trait locus, eQTL)的表达来自欧洲血统的个体[31]。PheWAS与eGFR的相关性最显著,两个snp rs10084572和rs77408001分别与大VLDL的身高和总胆固醇相关,但相关性不显著。
我们的研究有一些局限性,例如,糖尿病和高血压是肾脏损害的常见危险因素[32],然而,我们无法根据这些队列中潜在的患者肾脏疾病合并症(如糖尿病和高血压)进行分层分析。这将使我们能够确定哪些共病组对观察到的关联贡献最大。我们最大的贡献队列MVP先前报道了超过9k个具有32个全基因组显著变异的糖尿病分层GWAS个体[24]。他们报告说,在这项研究中发现的一个基因座SPATA5L1在非糖尿病组中具有最强的相关性。在本研究中,我们只能获得这些队列的GWAS汇总统计数据,没有社会人口统计学信息,因此无法进行本分析。
我们研究结果的另一个潜在限制是,在荟萃分析和MVP队列中,新型SNP rs77408001的效应量和标准误差都很大。我们主要将其归因于个体研究的不同表型转化。例如,UKBB是逆秩正态变换,MVP数据集没有变换,CKDGen数据集是对数变换。正是由于这个特殊的原因,我们进行了基于p值的元分析。
然而,另一个潜在的限制是,与新位点相关的SNP rs77408001的Imputation质量信息在两项研究的汇总统计中都无法获得。这一点,加上我们无法对该SNP进行直接复制分析,使得很难完全确认该SNP对非洲血统个体eGFR的真正遗传影响。我们建议将来进行类似设计的研究,以更详细地批判性地描述这种变异。
总的来说,我们的研究结果揭示了非洲血统个体中潜在的eGFR新位点,并进一步证实了先前在其他祖先中报道的那些位点。这里报道的一些变异是非洲祖先所特有的,因此这需要更大的特定于祖先的荟萃分析,以破译更多与非洲人CKD相关的位点。此外,我们在这里证明,即使是非洲以外的非洲血统个体也与非洲大陆人存在遗传差异,并且在进行GWASs时,应谨慎行事,不要一概而论。
百万老兵计划(MVP)
关于MVP队列的详细描述已在其他地方进行了描述[24]。简单地说,MVP队列从63家退伍军人医疗机构招募了完全同意的参与者。在记录的几种表型中,280722名参与者有eGFR分析。其中,57336人是非洲血统。大多数进行eGFR分析的参与者是非糖尿病患者,只有约33%为糖尿病患者。参与者进一步分为高血压和非高血压。约93%的高血压糖尿病患者是非西班牙裔黑人,但在该队列中,非西班牙裔黑人的eGFR通常高于非西班牙裔白人。我们纳入了MVP队列中所有具有eGFR的非洲血统的个体(n=57336),我们没有根据任何潜在的临床诊断对他们进行分层。关于这个队列的更多信息可以在补充方法中找到。
Chronic肾病遗传学(CKDGen)联盟
这是一个主要以不同种族的人群为基础的研究合作联盟。该联盟遵循集中分析计划,其中每个参与研究按照集中分析计划执行独立分析。根据参与者的年龄,CKDGen联盟的研究通常使用肾脏疾病研究方程中的四变量饮食修正[8]或Schwartz方程[33]来估计基于血清肌酐的eGFR。异常值对eGFR值的影响通过平均为15和200 ml/min/1.73 m2来协调。关于该研究的进一步信息,可以在http://k1.fpubli.cc/file/upload/202309/01/tywlphpijcj上找到,我们的研究中包括的参与者。[8]。这项研究招募了16474名非洲血统的参与者,并进行了eGFRcrea分析。关于CKDGen联盟的更多细节可以在补充方法中找到。
英国生物银行(UKBB)
UKBB是一项大型前瞻性队列研究,有超过5万名年龄在40-73岁之间的参与者。在之前的其他文献中已详细描述了入组过程中所遵循的步骤[20,23]。在基线时,每个参与者都完成了一份详细的电脑调查问卷。对存档血样进行生化试验和基因分型。对于纵向随访,研究数据与参与者的国家健康记录相关联。表型扩增仍在进行中。根据CKD-EPI方程计算基于血清肌酐的肾小球滤过率[34]。从UKBB队列中,我们的研究包括6217名非洲血统的个体,分析了eGFRcrea。补充方法有关于该队列的进一步详细信息。根据调查问卷,种族分为白人、黑人、南亚人或其他。然而,为了计算eGFR,种族被编码为黑人或其他。
我ta-analysis
由于个别研究应用了不同的GWAS特征转换[35],我们通过执行在metaL中实现的Stouffer方法来汇总汇总统计数据。其中两个数据集(UKBB和MVP)的基因组坐标在构建GRCh37/hg19中。本分析中使用的CKDGen数据集的基因组坐标在b36中报道,但在meta分析之前被转换为GRCh37/hg19。简而言之,该方法将双侧p值转换为反映参考等位基因关联方向的z统计量。然后对每个z分数进行加权;选择权值的平方之和为1,每个队列特定的权值与该队列中足够数量的平方根成正比。然后对三个队列的加权z统计量求和,并将汇总z得分转换为双侧p值。我们在特定研究分析中进行了两次GC校正,并重复meta分析的统计数据。单个数据集的问答图和meta分析在补充数据中给出。
精细定位
我们使用贝叶斯方法对8个先导snp的500kb内的所有snp进行精细绘制[36]。这种方法在其他地方有详细介绍[36]。简而言之,我们使用第i个SNP (Zi)的z得分来计算支持关联的贝叶斯因子,记为BFi,使用下面的公式(i):
(1)
K是研究的次数。
第i个SNP的后验概率(PP)使用下面的公式(ii)计算;
(2)
式中为该位点的snp总数。将snp按降序重新排列后,利用贝叶斯因子得到99%可信集。我们只计算后验概率≥0.99的snp。
FUMA分析
为了对每个先导SNP进行基因注释和功能定位,我们使用了一个名为fua的基于网络的平台。该资源利用来自多种生物资源的信息,促进GWAS结果的功能注释、基因优先级排序和交互式可视化[37]。
PheWAS分析
我们利用全球GWAS ATLAS资源对先导snp的功能进行了表征[38]。该资源汇编了28个域中超过3000个独特特征的超过4k个GWAS结果的目录。利用这一资源,对于每个先导SNP,我们评估了这些变异的遗传性质,包括效应大小分布、次要等位基因频率和与先导变异相关的性状的生物学功能。我们还描述了性状相关位点和相关基因的多效性程度,并研究了性状多基因性和SNP遗传力。
MAGMA基因集分析
使用MAGMA进行基于p值的基因集分析[39],该工具是funa中的一种工具。该方法对蛋白质编码基因进行基于基因的p值分析,通过将snp定位到位于相同基因中的基因。默认的MAGMA设置使用一个SNP-wise模型进行基因分析,一个竞争模型进行基因集分析。多重测试使用Bonferroni校正用于基因分析,FDR校正用于基因集研究。
eQTL分析
我们利用四个公开的肾脏eQTL资源:GTEx[31]、NephQTL[26]、Human kidney eQTL Atlas和RegulomeDB进行表达定量性状位点分析。对于每个导联SNP,我们分别在GTEx、NephQTL和Human kidney eQTL图谱中搜索与每个导联SNP相关的eQTL,包括肾皮质、肾小球和小管间质肾组织、全肾、肾小球和小管。我们使用RegulomeDB来确定每个导联SNP的调控影响。
动力分析
使用metaGAP软件估计p < 5 × 10-8的全基因组显著性的能力[40]。该工具的链接可以在http://www.devlaming.eu/metagap.html上找到。对于遗传关联分析,在严格的全基因组显著性水平(p < 5 × 10-8)下,约80,000个体的荟萃分析将达到80%的能力,以检测解释eGFR变异0.05%的常见遗传变异的关联(p < 5 × 10-8)。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12864-023-09601-0.pdf








