质谱法已被广泛接受为一种验证工具,用于敏感检测未申报的过敏原成分的存在。到目前为止,已经开发了多种方法,实现了不同水平的灵敏度和鲁棒性,但仍然缺乏分析验证的一致性和结果的可比性。在本研究中,内部验证了一种定量方法,用于确定巧克力基基质中的六种致敏成分(牛奶、鸡蛋、花生、大豆、榛子和杏仁)。后者已在食品试验工厂生产,以根据官方指导方针提供真实和特征良好的矩阵,以适当评估方法性能特征。特别是,欧洲标准化委员会最近发布的考虑事项已被遵循,以指导严格的单实验室验证,并具有主要方法性能,如选择性,线性和灵敏度。合成的肽标记物的替代物分别在基质匹配的校准曲线中以天然和标记的形式用作外部校准剂和内部标准。研究了两个数量级范围,重点关注低浓度范围,以便通过严格的校准方法正确评估检测和定量限(LOD和LOQ)。首次确定了所有六种致敏性成分的转换因子,以每质量食品中总致敏性食品蛋白(TAFP)的百分比(μgTAFP/gfood)报告最终定量信息,因为这样的报告单位可用于致敏性风险评估计划。除鸡蛋和大豆外,该方法的定量标记限略高(分别为1.1μgTAFP/gfood和1.2μgTAFP/gfood),其余成分的LOD值均在0.08 ~ 0.2μgTAFP/gfood之间。在接近目前可用的阈值剂量的四种定义浓度水平下,对巧克力棒的不同样品进行了分析,以测试分析方法的定量性能,并对不同变异性来源的测量不确定度进行了适当的估计。所达到的敏感性使其符合世界范围内发布或建议的各种阈值剂量。
近几十年来,质谱法(MS)已成功应用于食品中过敏原的检测和定量[1]。该方法具有明确的过敏原识别和固有的多路复用能力,为食品过敏原分析提供了一种参考方法。虽然使用合成肽作为外部校准剂代表了绝对蛋白质定量的金标准,但在致敏性食品测定的情况下,它提出了一个挑战,即检索数学因子,将LC-MS方法准确报告的肽含量转换为适当的单位,从风险评估的角度来看,这可以被认为是相关的。事实上,用于描述过敏原阈值的作用水平以总过敏原食物蛋白的毫克来表示,因为后者是触发免疫不良反应的食物部分[2]。迄今为止,针对这一关键问题的研究报道很少,但仅限于三种致敏食物,即牛奶、鸡蛋和花生[3,4,5,6,7,8]。理论方法[3,4,5]和实验方法[6,7,8]都得到了不同的结果,有时由于精心策划的蛋白质组序列的可用性有限,几乎没有可比性。此外,在过去10年中发表的针对多种致敏性食物的多种质谱方法显示出一些缺陷和局限性,因为报告单位缺乏共识,无法用于最终定量测定致敏性食物总蛋白[9,10,11,12,13,14,15,16,17]。这也适用于一些内部验证的基于质谱的敏感方法,其结果是过敏原发生率表示为每种食物中全部过敏原成分的质量分数[17]。
在此框架下,ThRAll (Thresholds and Reference method for Allergen detection)项目的主要目标之一是开发一种原型定量参考方法,用于在难以分析的食物基质中多重检测食物过敏原[18]。其中,选择巧克力和肉汤粉作为代表性复合食品,选择牛奶、鸡蛋、花生、大豆、榛子、杏仁等6种致敏食品作为目标食品[19,20,21]。这两种模型生成的食物基质是专门为食品试点工厂的项目目标而生产的,以模拟真实的生产过程,并在均匀性和稳定性方面进行了仔细的表征,以提供用于方法开发和验证的标准化材料[22]。先前的研究旨在开发多种过敏原分析方法,使用牛奶巧克力和黑巧克力作为模型基质[23,24,25,26],但发现过敏原标记肽的回收率很低且不令人满意。在类似应用中的进一步努力揭示了在具有挑战性的基质中适当优化提取、纯化和消化步骤的关键点,其中蛋白质可能与多酚和单宁结合[8,27,28,29]。我们关于巧克力分析样品制备方案优化的初步结果已于近期发表[30]。该方案在两个独立的实验室使用不同的三重四极柱LC-MS平台开发和测试,以确认其稳健性和可靠性。
在本次调查中,上述方法的内部验证已根据目前可用的官方建议和指南[31,32,33,34]完成。特别是,CEN发布的关于开发基于质谱的方法来测定作为致敏食品标记的蛋白衍生肽的主要分析要求的考虑[34]。用合成的原型标记物和同位素标记的类似物制备基质匹配校准曲线(MMCC)。通过MMCC线性回归与标准校准曲线(SCC)的统计比较,评价基质效应对检测灵敏度的影响。评估方法的灵敏度和线性度,并根据最严格的校准方法计算检测/定量限[34]。本研究采用发现致敏食物蛋白质组学的实验方法,确定6种目标食物中不同亲本蛋白的比例。计算出的转换因子用于确定4个发生的巧克力样品中6种致敏食物的绝对含量,分别添加了2、4、10和40μgTAFP/gfood浓度水平(食品基质中总致敏食物蛋白的质量分数)。与致敏性食物含量测量相关的总体标准不确定度是结合分析方法的各种变异性来源的贡献来估计的。当报告的定量标记/转换结果等于或大于相关的定量限制时,计算致敏食物的确定含量及其扩展不确定度。最后,对相同测试样品的精密度进行重复性和中间精密度评价。从内部验证中获得的结果已在以下章节中进行了批判性讨论。
胰蛋白酶金质谱级产品购自Promega(米兰,意大利)。溶剂和其他试剂购自Sigma-Aldrich(米兰,意大利)和VWR International PBI(米兰,意大利)。醋酸纤维素注射器过滤器,5 μm(尺寸25 mm),购自Sartorius Italy S.r.l (Muggiò, MB, Italy)。一次性脱盐盒PD-10购自Cytiva, GE Healthcare Life Sciences (Milan, Italy)。Strata-X聚合物反相(33μm;30毫克;1毫升;8B-S100-TAK)购自Phenomenex srl(米兰,意大利)。
定制的AQUA合成肽从Thermo Fisher Scientific (Life Technologies, Monza (MI), Italy)购买,作为天然序列(以下称为“轻”肽)和同位素标记类似赖氨酸(+ 8 Da)或精氨酸残基(+ 10 Da)(以下称为“重”肽)。轻肽要求为AQUA QuantPro级:纯度> 97%,在5% (v/v)乙腈/水中以5 pmol/μL浓度的标准溶液中配制1 nmol等分,浓度精度25-30%(通过氨基酸分析评估)。重肽要求为AQUA基本级:纯度> 95%,配方为单批冻干。
在5% (v/v)乙腈/水中,将各标记物等量混合至终浓度为312.5 fmol/μL,制备光肽混合物(SLM)原液。同时制备了100 fmol/μL的SLM_D工作稀释液。以冻干粉形式购买的每批重肽,以终浓度为100 pmol/μL悬浮在5% (v/v)乙腈/水中。在5% (v/v)乙腈/水中,将各标记物等量混合至终浓度为6.25 pmol/μL,制备重肽混合物(SHM)原液。制备了625 fmol/μL的工作液(SHM_D)。
根据需要对所有制备好的原液进行报价,并保持在- 20°C,直到使用,以避免重复冻融循环。选用工作溶液SLM (312.5 fmol/μL)、SLM_D (100 fmol/μL)和SHM_D (625 fmol/μL)进行选择性实验和制备校准曲线。
该方法验证应用于ThRAll项目中生产的模型食品矩阵(巧克力棒)[18]。这种基质是在食品中试工厂生产的,以模拟真实的生产过程[22]。巧克力在牛奶、鸡蛋、花生、大豆、榛子和杏仁的五种名义浓度水平下产生,即每克食物基质中总过敏原食物蛋白(TAFP)为0、2、4、10和40μg。巧克力样品制作成5克巧克力片,单独包装在密封的铝层压板中,保存在4°C直到使用。采用ELISA法在2g液相上评价样品的均匀性,并评价样品在整个方法开发和验证过程中的稳定性。关于模型食物基质生产和表征的完整描述可以在其他地方找到[22]。
空白和产生的巧克力样品进行了优化的样品制备方案,该方案在最近的一篇论文[30]中有详细介绍,并在在线资源中进行了总结(图S1)。简单地说,三个巧克力棒(大约15克)被实验室的搅拌器小心地磨碎,在冷藏条件下避免融化,并用1毫米的筛网筛过。用20 mL Tris HCl缓冲液(200 mM Tris·HCl, pH 9.2,含5 M尿素)在室温下(250转/分)剧烈搅拌30分钟,提取2g磨碎样品,然后在浴中超声15分钟。离心后收集上清,用5μM醋酸纤维素注射器过滤器过滤。过滤后的萃取物在一次性PD10脱盐柱上用粒径排除层析(SEC)纯化,用碳酸氢铵50 mM预处理,根据生产商自旋方案。在热变性、化学还原和烷基化后,取600μL的洗脱部分进行16 h的色氨酸消化[30]。将得到的消化液离心,取出500μL的等分液,转移到干净的微离心管中进行合成多肽标记。所有巧克力样品(空白和发生)加入一定量的重肽混合物(20μL SHM_D加入500μL消化基质),为所有肽标记物提供内标。此外,空白巧克力消化液也加入了越来越多的轻肽(工作溶液SLM和SLM_D)用于校准(详见“标准和基质匹配校准曲线的制备”)。
加标后的样品在Strata-X?一次性药筒上进行固相萃取(SPE)纯化(见图S1),预浓缩倍数为5,并通过HPLC-MRM进行分析。
将空白巧克力消化液(500μL)分别加入一定量的轻肽混合物(SLM_D或SLM,取决于样品)和一定量的重肽混合物(20μL SHM_D),制备基质匹配校准曲线(MMCC)。在轻肽终浓度为0、0、5、1、1、5、2、3、5、10、25和50 fmol/μL和重肽终浓度为25 fmol/μL时设置10个校准点。得到的样品按照图S1报告的方案进行SPE和预浓缩。
通过在模拟消解溶剂的碳酸氢铵溶液中加入越来越多的轻肽混合物(SLM_D或SLM,取决于样品)来制备标准校准曲线。在1-50 fmol/μL范围内制备了7个校准点,并按照为巧克力样品设计的相同方案进行SPE和预富集纯化。
除另有说明外,MMCC和SCC均进行HPLC-MRM分析,重复3次。最低检测点(0.5和1 fmol/μL)的精度也分别通过5次和10次生物重复进行评估。
对“巧克力棒的生产和样品制备优化方案”(0、2、4、10、40μgTAFP/gfood)中引用的已发生巧克力棒的测试样品进行分析,以进行精度评估。
对于分析方法的重复性评价,每个浓度水平制备3个独立的样品(生物重复),每个制备的样品获得3个仪器重复(技术重复)。对于中间精密度评价,在不同的日子(t=0,1,2,7)以40μgTAFP/gfood水平制备3个独立样本/天,由不同的操作人员(分析人员1和2)。此外,在不同的日子(t=0,7)以4μgTAFP/gfood发生水平在2个不同的日子(t=0,7)以3个独立样本/天测试中间精密度。
在证明分析反应无显著差异的情况下,对平均L/H比值值(日内和日内)进行肽含量的绝对定量。根据简化式(1),将报告的多肽含量换算为巧克力中总致敏食物蛋白(μgTAFP/gfood),通过MMCC回归参数()计算为fmol/μL:
(1)
在哪里
x 0,肽 :
多肽含量由MMCC插值测定,单位为fmol/μL。
cMM 蛋白质 :
中心摩尔质量(MM)报告单位为g/mol,并计算为目前已知的所有已测序的亲本蛋白同种异构体/变体检索到的最大和最小MM的平均值。
cCF 蛋白质 :
中心转换因子(CF)通过对致敏成分的发现实验确定,并以独立样本计算的最大和最小CF的平均值计算。
米 :
(1)用于蛋白质提取的基质与溶剂的比例为1:10,(2)国际单位制前缀之间的转换。
d :
1.33,消解过程中使用的稀释系数。
与确定的过敏原含量(相关的总体标准不确定度()结合分析方法的各种变异性来源的五个主要贡献者[32]来计算:
1.
与方法精度相关的标准不确定度()计算为重复观测值的标准差除以,假设为矩形分布;技术复制和生物复制都考虑了仪器变异性以及样品制备(提取、纯化和消化)的整体变异性。
2.
氨基酸分析中与合成肽原液()的浓度精密度相关的标准不确定度由制造商报价为25-30%;对于保守方法,考虑最大报告值(30%),相对标准差除以,假设为矩形分布。
3.
与线性最小二乘回归线()相关的标准不确定度,计算为
(2)
式中b=回归线斜率;=回归残差的标准差;n=MMCC标定点数;P=测定样品的重复次数;=未知样品的平均L/H比;=MMCC范围的平均浓度;=MMCC的平均L/H比。
4.
考虑在UniprotDB中检索到的蛋白质序列(已知同种异构体/变体)的可变性,计算标记蛋白摩尔质量的标准不确定度()。极差计算为最大值与最小值之差,半极差除以计算为相应的标准不确定度,假设为矩形分布。
5.
转换因子()的标准不确定度在同一过敏原成分的独立样品上实验估计。极差计算为最大值与最小值之差,半极差除以计算为相应的标准不确定度,假设为矩形分布。
应用误差传播规律,将5个影响因子合并为整体标准不确定度()[17]:
(3)
根据实验数据的正态分布,计算每种致敏成分测定含量的扩展不确定度(),其置信度近似为95% [32]:
(4)
六种致敏成分(IREs)的原始提取物在“巧克力棒的生产和样品制备的优化方案”中描述的相同实验条件下制备,根据先前研究[22]中报道的成分蛋白质含量,假设提取率为100%,理论浓度为2 mgTAFP/ mextract。在50毫升离心管中收集2克等分的磨碎的空白巧克力棒。在其中一个空白等分中加入适量(40μL) IREs至终浓度为40 μgTAFP/gfood。这样的样品将被称为“加标前(SB)”。SB样品在室温下开放1小时,使溶剂蒸发,然后与未处理的空白样品一起在4°C下保存过夜。孵育后,根据优化的方案(“巧克力棒的生产和样品制备的优化方案”)并行处理空白和SB,空白巧克力样品在SEC洗脱后仅增加一个步骤,用前面描述的相同IREs加标,最终浓度为40μgTAFP/gfood。后一种加标样品将被称为“加标后(SA)”。SA和SB按照优化方案(“巧克力棒的生产和样品制备优化方案”)进行酶解纯化。用MMCC插值法定量测定样品中的SB和SA,并以测定含量的百分率作为定量标记上各致敏成分的方法回收率的估计。
HPLC-MRM分析采用UHPLC LX-50系统和QSight?220三重四极杆质量分析仪(PerkinElmer)进行。色谱柱为Brownlee SPP Peptide ES-C18 (2.1 × 150 mm;2.7μm;160 ?)在30℃下用二元梯度(a: 0.1%甲酸在水中;B: 0.1%甲酸乙腈)。应用的洗脱梯度如下(流量0.3 mL/min):在10%B恒定0-3 min,从10%B到35% B 3-28 min;从35% B到90% B 28-28.5;28.5-43 min,恒定在90% B;从90% B到10% B 43 ~ 43.5 min;43.5-60分钟恒定在10% B进行柱平衡。
质谱采集采用time - mrm(多反应监测)模式,采用正离子分析,Q1和Q3均采用单元分辨率,采集窗口宽度为2 min。电离源设定为:干燥气体(氮气):120(任意单位);热表面诱导脱溶(HSID?)温度:250℃;雾化器气体:300(任意单位);电喷雾V1: 4500;离子源温度:400℃。数据处理使用simple?3Q软件平台v. 1.6进行。通过直接输注致敏成分的测试样品(每种成分的独立蛋白质提取物的胰蛋白酶消化),初步对特定肽标记进行仪器调整。为每个标记选择四个过渡,并适当优化其隔离/激活电压(见在线资源表S1)。后一种参数同样适用于原生和同位素标记标记物的获取。
将所有标记的每个轻肽(L)及其重类似肽(H)的峰面积进行整合,并计算其比值(L/H),作为进一步评价的分析信号。
采用数据独立采集模式(DIA)在高分辨率MS平台上进行发现实验。使用四极- orbitrap?混合质谱仪(Q-Exactive Plus由Thermo Fisher Scientific-San Josè, USA),色谱分离在Acclaim公司的PepMap100, C18色谱柱(3 μm, 100 ?, 1 × 150 mm)上完成。根据与基质提取相同的方案,以2 mg/mL的理论蛋白质浓度制备每种致敏成分的独立蛋白质提取物的胰蛋白酶消化物[30]。由于这些测试样品的蛋白质含量较高,所生成的多肽混合物的纯化/预浓缩步骤被跳过。采用Full MS/DIA模式分析胰蛋白酶消化,每个样品6个重复。全质谱采集如下:显微扫描1,分辨率35 k, AGC靶1e6,最大注入时间55,扫描范围350-1350 m/z。采用Skyline v.21.1建立DIA的隔离方案(范围350-1350 m/z,隔离宽度50 m/z,边界2 m/z),并在仪器方法上上传相关的纳入列表,设置进一步的参数,如microscan 1,分辨率17.5 k, AGC目标2e5,最大进样时间50 ms,循环计数22,隔离窗口50 m/z, NCE步长27.30。原始数据由MaxQuant(默认设置的工作流)处理,用于序列鉴定和蛋白质相关定量[35]。搜索算法应用于从Uniprot (http://k1.fpubli.cc/file/upload/202308/31/gznffiedb4c)下载的定制数据库。于2021年10月26日访问)。参考蛋白质组(RP)检索了感兴趣的6个分类中的5个:
Gallus Gallus (RP: UP000000539,蛋白计数:43,710,最后更新于2004年12月);
甘氨酸max (RP: UP000008827,蛋白计数:74,863,最近更新2013年2月),
牛牛(RP: UP000009136,蛋白计数:37,508,最近更新2018年3月);
花生(RP: UP000289738,蛋白计数:97,595,最近更新于2019年1月);
桃李(RP: UP000327085,蛋白计数31934,最后更新于2020年1月)。
关于Corylus avellana分类(ID 13451),目前没有参考蛋白质组,所有可用条目均已下载(506个)。尽管缺乏参考蛋白质组,但CF计算的实验方法同样适用于榛子,以保持一致性;然而,作者想强调的是,榛子组的CFs必须被认为是暂时的,等待对整个蛋白质组有更深入的了解。
摘要
介绍
材料与方法
结果与讨论
结论
数据可用性
参考文献
致谢
作者信息
道德声明
补充信息
相关的内容
搜索
导航
#####
该方法的选择性是在方法开发和验证过程中需要评估的初步特征之一,以确保测量信号唯一地归因于感兴趣的分析物,并且不受其他干扰化合物的影响,从而导致测量偏差。对于基于质谱(MS)的检测,除了用于多肽分离的色谱条件外,整个方法的选择性与肽标记物的特异性以及食物基质的组成严格相关,这些成分可能在所选的MRM(多反应监测)窗口内产生干扰峰。
根据CEN指南,本研究中使用的标记物的特异性在硅和实验中都得到了证实[34]。在计算机评估方面,我们与网上可获得的主要蛋白质数据库进行了序列比对,结果发表在之前的研究中[36,37]。然而,由于只要更新公共数据库,这种计算机评估就可以提供新的结果,因此最近还通过蛋白质勘探者工具(MS-Homology工具[38])进行了进一步的检查,在最后发布的数据库中搜索色氨酸肽的100%一致性,确认了先前获得的结果(见表1)。
表1为质谱法选择的蛋白质和肽标记总结。整个论文中使用的肽编码已被报道。通过BLAST检索主数据库评估肽特异性2 .链接本文:2020.09.02,和swissprof .2021.06.18),使用门户网站MS Prospector上提供的MS- homology工具
此外,为了揭示由等压共渗化合物引起的基质本身的潜在干扰,对加入同位素标记肽的空白巧克力基质进行了分析,以评估测量信号中的干扰程度,从而在实验上确认选择性。在优化的色谱分离条件下,所获得的过渡段未检测到明显的干扰(见图S2)。然而,我们特别注意了肽mw-IDA的色谱分离,以避免具有强烈干扰带的特定信号重叠,同时影响458.7/688.4和458.7/504.2(见图S2)。
基于质谱的方法中致敏成分的绝对定量可以通过外部校准物来实现,例如天然合成肽的混合物、市售标准蛋白、整个成分或参考物质。根据所选择的校准器,管道的复杂性和与测量相关的总体不确定度可以改变。在这里,所选标记物的合成替代品被用作校准剂,并被同位素标记的类似肽标记物也被包括在内(见表1)。后者被用作每个分析运行的内部标准,并用于将从MRM获取获得的归一化峰面积(轻肽与重肽形式的比例)的测量转换为肽浓度。根据CEN指南的建议,将轻合成肽和重合成肽添加到固定数量的空白巧克力消化液中,以获得基质匹配校准曲线(matrix-matched calibration curves, MMCC),以补偿基质效应[34]。在固相萃取(SPE)纯化步骤之前进行校准剂和内标品的峰化,以使分析信号归一化,并将SPE的肽回收率和仪器波动(色谱分离和/或电离效率)对总体变异性的贡献最小化。
制备MMCC时,根据“制备标准和基质匹配校准曲线”的描述,在等分的空白巧克力消化液中加入越来越多的轻肽混合物和固定数量的重肽混合物。特别是,校准曲线考虑了较宽的浓度范围,涵盖了两个数量级,总共有十个校准点,包括空白样品,这大大超过了CEN指南规定的最低5个点[34]。大多数校准水平都有意选择在范围的第一部分,最高为5 fmol/μL,以便在最低响应时正确表征方法的性能。
作为第一步,在整个浓度范围内计算回归线,在所选水平上对所有标记物的检测一致。除蛋清肽ew-ISQ和ew-GGL峰仅从1 fmol/μL样品开始检测外(见表2)。拟合参数证明,在所研究的范围内,响应具有良好的线性关系(R2≥0,993),并且根据特定的致敏成分具有可变的灵敏度(见表2)。根据校准曲线斜率计算的灵敏度,选择一个标记物作为定量报告物(QTM,定量标记)对每种致敏成分(在牛奶和鸡蛋的情况下有两个,用于部分食品配方),而第二个标记被监测用于确认目的(QLM,定性标记)。
表2合成肽的基质匹配校准曲线计算方法对6种致敏成分的敏感性性能总结(天然肽的归一化信号为同位素标记肽)
通过比较MMCC与在模拟消化缓冲液的简单溶液中分析合成多肽混合物得到的标准曲线,评价基质组成对检测的一般影响。在相同的MMCC浓度范围内制备的标准溶液,按照已经描述的巧克力样品的方案进行SPE纯化和预浓缩,并进行HPLC-MRM分析。同样,计算轻重比,建立“标准”校准曲线(SCC),以提供一组与MMCC非常相似的数据,除了巧克力背景的存在。然后通过MMCC和SCC两条回归线的斜率进行统计比较(学生t检验)来评估矩阵效应。比较两条回归线的斜率是分析实验室中相当常见的任务;然而,文献在如何计算t检验统计量的汇总标准误差方面存在差异,在这种情况下,我们参考了2014年Andrade和est
- psamuz - psamuzi的综述[39]。为了选择和应用适当的t检验假设,通过Fisher-Snedecor的f检验对MMCC和SCC的回归方差(残差标准差,Sy/x)的相似性进行了首次初步筛选,即将最大方差除以最低方差,并将其与统一(单尾检验)进行比较。对于所有的qtm, MMCC和SCC的回归方差在1%的显著性水平上没有显著差异,允许将误差方差按其自由度加权,用于t检验执行。计算的t检验统计量证明,除ew-ISQ和mw-VLV外,所有定量标记的MMCC和SCC回归线的斜率在95%的置信水平上有显著差异。这些结果证实了制备MMCC对巧克力棒等复杂食品基质中残留致敏成分的适当绝对定量的相关性。
如前所述,特别注意表征方法在低校准范围内的性能,后者与追踪甚至少量的意外污染更相关。在0.5 ~ 5 fmol/μL范围内设置6个标定点,利用该数据集计算检出限(LOD)和定量限(LOQ)。根据定义,检测限是测试样品中可可靠地与空白区分开的分析物的最小浓度。尽管LOD的定义很清楚,但对LOD的实验评估却争论了很长时间;事实上,独立研究小组通常仍然使用不同的方法。我们的观点是,通过考虑在所调查的校准范围内(截距或残差的标准差(SD))或最低浓度水平下超过10个独立样本的校准方法来计算lod和loq,以避免过于乐观的结论[1]。在本研究中,我们计算LOD和LOQ分别为3和10倍的截距SD除以校准曲线的斜率。据报道,该方法对六种致敏成分(牛奶、花生、大豆、榛子和杏仁)中的五种具有非常好的均匀性,LOD值在0.1至0.2 fmol/μL之间,而ew-ISQ标记的LOD值略高,最高可达0.9 fmol/μL(见表3)。
表3最低检测点的方法精密度总结及低co校准法的检出限和定量计算矩阵匹配校准曲线(回归模型)的浓度范围(ew-ISQ≤25 fmol/μL,其他所有标记≤5 fmol/μL)y=bx +一个,SDa截距的标准差)
作为进一步的步骤,我们测试了该方法在最低检测点(LDP)的精度;事实上,除了用于计算检测/定量限的分析方法外,LDP的精度是方法可靠性评估的一个非常关键的点。性能非常令人满意,所有qtm的相对SD≤20%(见表3)。
为了提供方法灵敏度的完整概述,我们还计算了极限LOD和LOQ,并从(i)线性回归的残差SD和(ii)最低检测点的信号SD中对SD进行了替代估计。这些数据已被附加在在线资源的表S2中。作为一般性评论,基于截距或基于LDP sd的LOD/LOQ估计通常非常具有可比性,证实它们可以同样适用;然而,对回归残差计算的限制总是被高估,可能是由于更严格的分析方法,它包含了整个回归线的方差。
报告单位及conversion因素
合成肽作为绝对定量的外部校准剂的应用依赖于这样的假设:亲本蛋白在样品中被完全消化,标记肽的释放是等摩尔的,并且这些标记肽在消化过程中是稳定的。在该分析方法中,两种假设都在方法开发阶段得到了检验和确认[30]。因此,这种方法可以提供样品中标记肽量的准确定量。然而,为了从风险评估的角度传达可用的信息,需要将肽报告单位(RUs)首先转换为母体蛋白的mg,然后再转换为分析基质中的总致敏食物蛋白(TAFP)的mg。设计和应用数学因子将多肽转化为TAFP需要一些信息,其中一些信息很容易实现,因为与样品制备方案严格相关(即整个工作流程中的基质-溶剂比和稀释因子),其他信息则更为关键。特别是,两个主要信息,即亲本蛋白的摩尔质量(MM)及其在致敏成分总蛋白谱中的相对丰度(这里称为转换因子CF),可能是该方法不确定性的主要来源。
至于蛋白质的摩尔质量,重要的是要考虑到肽标记通常不是亲本蛋白所独有的,而是在蛋白质异构体/变体中共享的。这应该在不确定性预算中考虑,并且应该优先使用同工型之间的平均MM,以提高值的代表性。Martinez-Esteso等人[3]在最近的一项调查中首次报道了这些考虑,该调查涉及饼干中的牛奶测定,在这里,我们决定对所有六种感兴趣的致敏成分应用类似的方法。值得注意的是,牛奶可能是最广泛表征的食品成分,而其他五种成分(鸡蛋、花生、大豆、榛子、杏仁)的信息只有部分或非常有限。尽管如此,我们还是收集了目前已知的编码特定特征肽的所有可用的蛋白质标记(见在线资源的表S3)。分别计算最大和最小mm (cMM)之间的平均值和该范围的半宽除以,进行RUs和不确定性估计的数学转换()(见在线资源的“致敏成分量化和报告单位的转换”和“不确定性估计”及表S3)。值得注意的是,乳蛋白以外的标记蛋白的MM相对标准不确定度较低(≤0.6%),并不能反映结果的高可靠性,而主要是对蛋白质异构体/变异的有限了解。
RUs转换所需的第二个关键信息是CF。该信息可以通过理论方法[3,4,5]或实验方法[6,7,8]检索。理论方法需要对致敏食品成分的蛋白质谱进行定性和定量的了解,并提供平均估计,这更有可能广泛地代表自然变异性。然而,这种详细的知识目前只适用于牛奶、鸡蛋和部分花生;因此,对于大多数主要的致敏成分,理论上的方法还不是负担得起的。不同的是,实验方法依赖于在方法开发中使用的特定成分上进行的基于发现质谱的实验,通过光谱计数来确定不同亲本蛋白的比例。当获得的值用于测量多种致敏成分来源时,可能会引起一些担忧,这些成分来源的组成蛋白质的比例可能不同,但是,测试来自不同供应商的一组致敏食品可能是获得更具代表性的实验CFs的解决方案。实验方法的可行性也依赖于良好注释和整理的蛋白质组序列的可用性,因此,如果新的蛋白质组被收集、整理并在公共领域共享,则可以随着时间的推移而改变和改进。
从这一背景出发,并考虑到目前六种致敏成分中有五种参考蛋白质组的可用性(参见“转换因子计算的发现实验”),在本研究中,为了保持一致性,采用了转换因子计算的实验方法。
简单地说,每一种致敏成分的小份额用于生产所引起的巧克力棒已经提取了相同的缓冲液的方法,并消化胰蛋白酶。多肽池采用高分辨率质谱分析,原始数据通过软件处理进行蛋白相关定量(详见“计算转换因子的发现实验”)。针对每个致敏成分获得的数据集根据其自身的参考蛋白质组进行搜索,允许仅基于独特和剃刀肽的蛋白质定量。在得到的蛋白质和多肽列表中浏览选择的标记。分配给目标蛋白的强度,以及任何可加密相同肽标记的同种异构体/变体的强度,除以所有已鉴定蛋白的强度总和。这个比率被假设为过敏原成分中蛋白质相对丰度的实验估计。当多肽标记在一个以上的异构体/变体中检测到时,每个异构体由至少一个独特的多肽鉴定,所有材料的相对丰度之和被考虑用于CF计算。对所有重复应用相同的数学计算,在线资源的表S3报告了平均cf及其不确定性(k=1)。值得注意的是,目前对榛子的了解非常有限(见“转换因子计算的发现实验”),这可能严重影响实验计算得出的CFs的可靠性。然而,由于没有任何可行的替代方法来计算榛子的转换因子(无论是理论还是实验),我们决定处理从榛子中获得的发现数据,同样处理其他致敏成分,尽管意识到这一特定数据集的不确定性,作为临时解决方案,可能会在不久的将来更新。
据我们所知,这是第一次将CFs计算并应用于大豆、杏仁和榛子的绝对定量的研究;因此,无法与独立研究小组先前进行的调查进行批判性比较。然而,将我们的结果与以往的文献成果进行比较,可以得出一些关于牛奶、鸡蛋和花生的评论和结论。对于牛奶,我们的实验方法报告了α s1 -酪蛋白的CF为0.374,an为0.009 (k=1),这里选择α s1 -酪蛋白作为定量报告亲本蛋白。有趣的是,对于相同的标记蛋白,该值与Martinez-Esteso等[3]计算的理论值(0.366,an=0.046)并无显著差异(k=1)。相反,我们的实验方法导致β-乳球蛋白CF的高估,等于0.193,an为0.002 (k=1),而理论值为0.102,an为0.010 (k=1)[3]。值得注意的是,Parker等人[6]在2015年的论文中也观察到同样的实验方法对β-乳球蛋白CF的高估,报告的CF为0.178 (CF值没有不确定性;因此,无法提供适当的统计比较)。这表明,对于实验方法,结果的可靠性严格取决于特定的蛋白质性质(可提取性,消化率和胰蛋白酶的电离效率)。对于鸡蛋蛋白,文献中尚未提出CF的理论计算和相关的标准不确定度;然而,对鸡蛋组成和蛋白质谱的自然变异性有很好的了解。因此,我们可以将Martinez-Esteso等人[3]提出的相同方法应用于鸡蛋蛋白,得到卵白蛋白的理论CF为0.31,an为0.03 (k=1)(该计算的所有细节均在在线资源表S4中报告)。此外,在本例中,我们的实验方法提供了卵清蛋白CF 0.468的高估,误差为0.003 (k=1),这与Parker等人[6]在2015年报道的0.421的实验CF一致。同样,两种实验方法计算出的Ara h 3的CFs非常接近(0.695,误差为0.006 (k=1),误差为0.624[6])。
对所有致过敏成分计算的CF()的相对标准不确定度在1 - 8%之间,其中牛奶CF(5%)和大豆CF(8%)的不确定度最高(见在线资源中的表S3)。值得注意的是,根据其定义,这只说明了与用于CF实验估计的分析方法相关的变异性,而不包含有关致敏成分的蛋白质谱的自然变异性的任何信息。考虑到Martinez-Esteso等人[3]在论文中定义的牛奶的自然变异性,这个临界点证明了α s1 -酪蛋白计算的不确定性较低(5%),而报告值为13%。
考虑到基质与缓冲液的比例为1:10,在整个样品制备方案中使用稀释系数,以及适当的国际体系单位前缀,完成了从肽浓度到巧克力中TAFP(μgTAFP/gfood)的最终转换(方程式见“致敏成分定量和报告单位的转换”)。为了清楚起见,表S3列出了应用于每个报告的肽标记物的转换因子,并将这些因子用于转换之前在μTAFP/gfood报告单元中评论的LOD/LOQ值(见表3)。
产生的测试样品的绝对定量
该方法的定量性能在一家食品中试工厂的四个测试样品中进行了验证,并在均匀性和稳定性方面进行了很好的表征[22]。这些样品是巧克力棒(ICB)中每种致敏成分的规定水平,即2、4、10和40μgTAFP/gfood,以食物基质中致敏成分总蛋白的质量分数计算。对每个浓度水平进行生物重复和技术重复分析,并利用记录的分析信号通过MMCC插值报告多肽标记物的含量。根据式(1)将测定的多肽含量转化为食品基质中致敏成分的总蛋白。当检测到至少两种多肽的至少两次过渡并定量高于特定lod时,即认为ICB中致敏成分检测成功。每当报告的定量标记/转换结果大于或等于相关定量限时,即可完成成分含量的定量。
根据公式(3)计算每个确定含量的总体标准不确定度,并结合五个主要因素作为与(i)方法精度(),(ii)合成肽储备液浓度精度(),(iii)线性最小二乘回归线(),(iv)蛋白质标记物分子量()和(v)转换因子()相关的变异性来源。为了清晰起见,在图S2中,五个贡献因子被报告为每个测试样品(ICB 2-40μgTAFP/gfood)的相对标准不确定度()。值得注意的是,不确定度,和相等地计算在所有测试样本上,而两者都是样本依赖的。特别是,公开了与所有测试标记物的发生水平成反比的比例。此外,为40μgTAFP/gfood ICB样品制备的高重复次数(p值在式2中)通常接近校准范围的上限,也有助于在该水平上保持较低的水平。此外,由于该不确定度值受多个因素的影响,例如特定标记物的敏感性以及测定多肽含量的平均生物和技术重复次数,这些因素在不同的测试样品中有所不同,因此结果具有样品依赖性,但没有观察到一般趋势。所有这些结果和考虑表明,得出总体方法不确定性的主要贡献者的一般结论是一项相当具有挑战性的任务,因为它取决于无数因素,包括操作员,校准范围,重复次数,特定标记物的敏感性以及对致敏成分蛋白质谱的了解。因此,考虑到所有可能的贡献者将是最好的保守的方法,一个最自信的论文。
最后,通过考虑覆盖因子,计算所有定量标记/过渡的扩展不确定性,置信水平近似为95%[32]。每种致敏成分的测定含量及其扩大的不确定度见图1和表S5。综上所述,在ICB样品(2-40μgTAFP/gfood)的所有测试浓度水平下,该方法成功地定量了牛奶、榛子和杏仁。对花生也证明了满意的结果,其中从4 ppm ICB开始完成了定量。对鸡蛋和大豆的敏感性稍低,其中只有两个最高的ICB(10-40μgTAFP/gfood)被量化。
图1
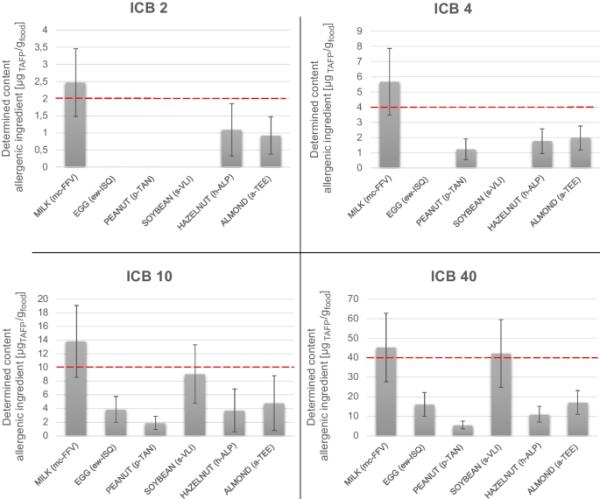
在4个浓度水平(2、4、10、40μgTAFP/gfood)下,获得了相关的组合不确定度和扩展不确定度(k=2)的定量结果。根据表S3所载的因子换算报告单位,以每食物基质中总致敏食物蛋白的质量分数报出测定的浓度
精度
在同一实验室ICB中评估所有浓度水平(2-40μgTAFP/gfood)的重复性。3份独立样品由同一操作人员在同一天、相同条件下制备,采用LC-MRM进行分析,并进行3次技术重复。每个定量标记物的轻重比采用95%置信水平的单因素方差分析进行比较,三个生物重复在每个浓度水平上没有显著差异,因此可以在同一天内汇集所有数据。所有定量标记的日内变异系数(CV%)结果非常令人满意,始终低于15%,与测试的浓度水平没有任何特定的相关性(见表4)。关于仪器分析(IA)和样品制备(SP)对总体方差的相对贡献,作为一般趋势,可以观察到IA是最低检测水平的主要贡献者,即牛奶(酪蛋白酸盐)的2μgTAFP/gfood ICB;榛子和杏仁,花生4μgTAFP/gfood ICB,鸡蛋(蛋白)和大豆10μgTAFP/gfood ICB。相反,除鸡蛋和大豆外,所有QTM的SP贡献在最高测试浓度(ICB 40μgTAFP/gfood)下普遍存在(见表4),这与这两种致敏成分的较低敏感性一致。
表4 e方法重复性和中间精密度评价:测定的多肽co的相对标准偏差(CV%)含量(fmol/μL)“样品制备(SP)”、“工具分析(IA)”、“分析日(DA)”和“分析师(A)”对总方差的贡献
此外,在ICB样品可用的四个浓度水平中的两个水平上评估了中间精度,选择了中低(4μgTAFP/gfood)和高(40μgTAFP/gfood)测试样品,仍然覆盖浓度的一个数量级。这组实验改变了操作人员和分析日期。同样,在不同条件下获得的平均值通过95%置信水平的单因素方差分析检验进行比较,结果显示没有显著差异。然后对获得的数据进行平均,结果非常有希望,除了β-乳球蛋白报告标记(29%)外,CVs始终低于15%。特别是,中间精度导致5 - 11%范围在4 ppm测试级别,在8 - 15%的区间40 ppm水平测试(见表4)。至于不同因素对总体差异的相对贡献,普遍来源导致SP和天的分析,而运营商似乎总是一个较小的因素除了鸡蛋和大豆成分,在权重似乎均匀分布的三个因素。
样品随时间的稳定性
除了上一段描述的精度评估外,还设计了一个特别实验来评估在短时间内(3天)产生的分析样品的稳定性,并提供该方法性能特征的完整描述。
特别地,这种评价是在一组独立的ICB样品(40μgTAFP/gfood)上进行的,一式三份,在同一天和三个不同的日子(总共9个生物样品)制备。每个样品在同一天分析3次(第0天进行技术重复),然后在接下来的2天再次分析,将样品保存在+ 8°C冷藏(第1天和第2天分别记录2个技术重复)。各定量标志物当日及3天内的平均值采用5%显著性水平的t检验进行比较。结果证明,每个独立样品中所有标记物计算的平均值在所有制备的独立样品中没有显著差异,从而证实了样品在受控冷藏条件下超过48 h的稳定性。
根据CEN指南[34],通过加标样品的回收率计算来评估分析方法的准确性。特别是,空白样品在样品制备方案的不同阶段用致敏物的蛋白质提取物加标以进行比较(“在SB之前加标”和“在SA之后加标”,详见“真实性/回收率实验”)。通过MMCC插值法对SB和SA样品进行定量,并以测定含量的百分比作为QTM上每种致敏成分的方法回收率的估计。结果严格依赖于特定的QTM和致敏成分,总体上仍然令人满意。事实上,乳肽标记的回收率分别为80% (m-FFV)和87% (m-VLV),鸡蛋标记的回收率分别为100% (ew-ISQ)和97% (ey-ATA),花生标记的回收率分别为53% (p-TAN)、40% (s-VLI)、64% (h-ALP)和73% (a-TEE)。花生和大豆标记物的加标回收率较低;不过,将进行进一步调查以解释这些证据。
如前所述,在评估交叉污染的影响和做出有关适当的过敏原管理和标签的决策时,实现RUs的这种转换符合将方法性能特征与定量风险评估相关联的需要。在这个框架下,最初由澳大利亚和新西兰过敏原局创建的自愿附带微量过敏原标签(VITAL)计划提供了一个有用的系统,也被欧盟的许多国家所考虑[2]。特别地,VITAL项目根据可获得的临床数据建立了参考诱导剂量(EDs),用于保护至少95% (ED05)或99% (ED01)的过敏人群。VITAL计划的最新3.0版本于2019年10月发布,它为行动水平1设定了以下参考剂量(TAFP毫克):牛奶、鸡蛋和花生0.2毫克,大豆0.5毫克,榛子和杏仁0.1毫克。低于这个阈值,不需要预防性标签说明,99%的过敏人群可以安全食用这些食物。在欧盟内部没有相关法律机构发布的其他官方和统一限值的情况下,一些国家,如德国、荷兰和比利时,发布了目前在其境内推荐的参考剂量,而邻国之间的参考剂量差异很大(见表5)。联合国粮食及农业组织(粮农组织)和世界卫生组织(世卫组织)联合开展了一次关于食品过敏原风险评估的专家磋商,最近发表了关于审查和确定重点过敏原阈值水平的结论(见表5)[40]。以这里分析的六种过敏原为重点,该文件显著提高了先前推荐的鸡蛋和花生的阈值至2.0毫克,榛子至3.0毫克,杏仁至1毫克(后者是临时值),而牛奶的修订阈值仍有待确定。
表5目前世界范围内推荐或发布的食物过敏原参考剂量(RD)[总致敏性食物蛋白毫克]的总结,以及与本方法评估的定量限值的比较;有限公司对绝对总致敏性食物蛋白[mg]的定量限进行了反演考虑到巧克力棒的份量(PS)为25克
为了与这些行动水平进行直接比较,考虑到巧克力棒的合理分量为25克(见表5),验证方法所达到的检测限被转换为绝对数量。值得注意的是,所获得的灵敏度性能远远高于所有发布/推荐的限值,除了荷兰立法,与其他官方文件相比,荷兰立法似乎不切实际地严格。
下载原文档:https://link.springer.com/content/pdf/10.1007/s00216-023-04894-2.pdf








