子宫内膜癌的分子亚型与生存结局显著相关,可以指导手术方法和术后辅助治疗。其中TP53mut亚型预后最差,需要术后检测才能确定。因此,确定术前无创临床参数,早期预测TP53mut亚型,对临床医生选择合适的手术方式和早期预警具有重要的指导意义。本研究旨在利用子宫内膜癌术前无创参数,建立早期预测TP53mut亚型的模型,筛选出潜在的TP53mut患者。
收集2011年6月至2020年7月北京大学肿瘤医院妇科FIGO I-IV期子宫内膜癌376例手术患者资料及病理标本,最终纳入178例病例作为训练数据集(part A)。收集2022年1月至2023年3月的36例病例作为验证数据集(part B)。采用一站式下一代测序(NGS)方法进行分子分型。与TP53mut亚型相比,POLE EDM、MSI-H和TP53野生型亚型被定义为非TP53mut亚型。采用单因素Cox回归分析和多因素logistic分析确定与TP53mut亚型相关的术前临床参数。采用术前无创参数建立nomogram预测模型,验证其预测TP53mut亚型及生存结局的有效性。
多因素logistic回归分析显示,HDL-C/LDL-C水平、CA125水平、宫颈或下子宫受累是与TP53mut亚型相关的独立影响因素(p=0.016、0.047,<0.001)。根据多因素分析确定的因素构建TP53mut预后模型(TPMM),即A部分TPMM=-1.385 × HDL-C/LDL-C + 1.068 × CA125 + 1.89 × CI或LUI, AUC=0.768 (95% CI, 0.642 ~ 0.893), B部分TPMM预测TP53mut亚型的AUC为0.781(95% CI, 0.581 ~ 0.980)。根据A部分的模型预测,TP53mut亚型患者的无进展生存期(PFS)和总生存期(OS)明显差于非TP53mut亚型患者。
TP53mut预测模型(TPMM)具有较好的诊断准确性,生存分析表明该模型可以识别不同预后风险的患者。
子宫内膜癌是最常见的妇科恶性肿瘤,其发病率呈逐年上升趋势。在全球范围内,1990年至2019年期间,EC的年龄标准化发病率每年增加0.69%[1]。过去,EC被分为I型和II型。病理类型称为I型EC,主要是子宫内膜样癌,依赖雌激素。其他病理类型,如浆液性癌、透明细胞癌和混合性癌,不依赖激素,预后较差,称为II型子宫内膜癌[2]。然而,这些分类和临床结果之间存在很大的不一致性。为了解决这一问题,2013年的The Cancer Genome Atlas (TCGA)基于EC的综合基因组特征,定义了4个EC预后亚群:POLE突变型、MSI-H型、低拷贝型和高拷贝型[3]。该分子分类系统与临床结果一致;也就是说,POLE超突变肿瘤具有良好的无进展生存期,MSI-H和低拷贝肿瘤具有中等的无进展生存期,高拷贝肿瘤具有较差的无进展生存期。这四类分子分型系统与预后有较好的相关性,目前被认为是子宫内膜癌分子分型的金标准。然而,TCGA分子分型系统由于操作复杂、检测成本高,难以广泛应用于临床。因此,学者们提出了Proactive Molecular Risk Classifier for endomecancer (ProMisE)方法[4]和TransPORTEC方法[5]来完善TCGA分子分型体系,所获得的预后信息与TCGA分子分型体系基本一致;即与POLE高突变型肿瘤相关的预后最好,与MSI-H和TP53野生型/无特异性分子谱(NSMP)肿瘤相关的预后为中等,与TP53突变型肿瘤相关的预后最差。尽管近年来分子分型已被临床医生广泛接受,但无创方法预测子宫内膜癌亚型多采用机器学习方法[6,7],而基于术前临床参数建立模型预测EC分子亚型的临床研究较少。
模态图是一种图形预测模型,通过分析多个定量和定性变量来预测特定事件的概率。它可以用来说明单个病人的风险。该模型基于logistic回归和Cox回归,并以可视化的方式呈现结果。根据模型的回归系数制定评分标准,并为每个自变量赋一个分数。然后,通过转换函数计算每个患者的结束事件的概率。Nomogram预测模型已被用于预测几种肿瘤的复发、转移和生存结果[8,9,10,11],但用于预测EC风险的模型报道较少。
本研究旨在建立基于一站式新一代测序(NGS)方法的nomogram预测模型,利用术前临床参数预测临床预后最差的TP53mut亚型,并在手术前提供疾病状态信息,帮助临床医生制定合适的手术方法和术后辅助治疗。
本研究经北京肿瘤医院伦理审查委员会批准,参考文献号2021YJZ21,并按照《赫尔辛基宣言》的指导原则进行。所有参与者在采集样本时都提供了书面知情同意书。本研究包括两部分患者:A部分(训练数据集)用于探索术前预测因素,建立预测TP53mut亚群的模型;B部分(验证数据集)用于验证A部分的模型。A部分:收集2011年6月至2020年7月北京大学肿瘤医院妇科FIGO I-IV期EC手术的376例患者的资料和病理标本,最终纳入178例。B部分:收集我中心2022年1月至2023年3月63例患者资料及病理标本,最终纳入36例。患者入组过程如图1所示。
图1
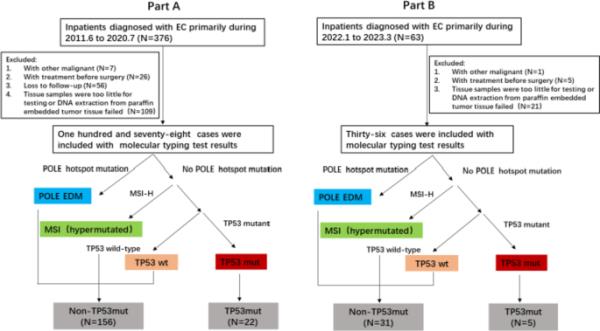
患者入组过程和一站式NGS分子分型程序
标准手术范围包括全子宫切除术和双侧输卵管-卵巢切除术。选择患者行淋巴结切除术。所有患者术前均未接受放化疗或激素治疗。两名妇科病理学家检查病理标本。提供1 mm直径的外科肿瘤标本,至少15张载玻片用于测序。辅助治疗根据手术分期和组织学类型量身定制。高危子宫内膜样癌患者接受阴道近距离放疗或全盆腔放疗。阴道近距离放疗主要局限于接受手术淋巴结评估的患者。非子宫内膜样癌或晚期子宫内膜样癌患者采用化疗和放疗联合治疗。紫杉醇联合卡铂是标准的化疗方案。
收集术前一般特征、血液学及影像学检查结果、病理特征、术后辅助治疗结果及生存随访结果。中性粒细胞、单核细胞、淋巴细胞、血小板、血红蛋白按血常规平均值±SD × 109/L计算。比率数据按中位数分组,将血液生化结果分为低于参考范围、在参考范围内、高于参考范围三类。肿瘤生物标志物分为参考范围内和参考范围以上两类。图像数据由两名具有10年以上工作经验的放射技师确定。
肿瘤组织的基因组分析使用oncoScreen Plus面板的520个癌症相关基因。使用QIAamp DNA FFPE组织试剂盒(Qiagen, Hilden, Germany)按照制造商的标准方案(Qiagen, Hilden, Germany)从福尔马林固定石蜡包埋(FFPE)肿瘤组织中提取组织DNA。利用520个基因面板(oncoScreen PlusTM, Burning Rock Biotech, Guangzhou, China)进行捕获靶向测序[12,13,14]。数据分析包括变量调用和解释、拷贝数变化、肿瘤突变负担(TMB)估计和微卫星不稳定性(MSI)状态评估。非整倍性评分是使用先前报道的获得或丢失的染色体臂的总数来计算的。在本研究中,只有极外切酶结构域密码子286、297、411、456和459的极热点突变被认为是超突变的原因突变,并被定义为POLE EDM亚型。患者分为4个分子亚型:POLE EDM、MSI-H、TP53野生型和TP53mut。在本研究中,与TP53mut亚型相比,将POLE EDM、MSI-H和TP53野生型亚型定义为非TP53mut亚型。A部分和B部分的一站式NGS分子分型流程如图1所示。
一站式NGS分子分型流程如下:小组对子宫内膜癌患者存在的突变基因进行分析,根据突变结果对患者进行逐个分类。首先,对肿瘤进行聚合酶e (POLE)外切酶结构域突变(EDMs)评估。其次,评估MSI超突变。第三,根据肿瘤是否存在TP53突变,评估TP53突变亚型和TP53野生型亚型。本研究对TP53mut组和非TP53mut组(包括POLE EDM、MSI超突变和TP53野生型)进行了重新分类。
所有患者术前2年每隔3个月随访一次,术后3年每隔6个月随访一次,术后5年每隔1年随访一次。记录疾病进展和死亡情况。无进展生存期从手术日期计算到疾病进展发生的数据或在最后一次随访日期进行审查。总生存期从手术之日起计算至死亡或最后一次随访之日止。进展定义为局部或远处复发或死亡。
所有统计分析均使用R软件(4.1.2版本)和SPSS软件(22.0版本)进行。TP53mut组与非TP53mut组的分类变量差异比较采用卡方检验或Fisher精确检验,连续变量比较采用因变量t检验或Mann-Whitney检验。采用多因素logistic回归分析筛选识别TP53mut患者的独立因素,建立预测模型,生成nomogram。绘制受试者工作特征(ROC)曲线,计算曲线下面积(AUC)、敏感性和特异性。采用Kaplan-Meier曲线和log-rank检验比较模型预测TP53mut组和模型预测非TP53mut组的无进展生存期和总生存期。双侧p < 0.05认为有统计学意义。
摘要
背景
方法
结果
讨论
结论
数据和材料的可用性
缩写
参考文献
致谢
作者信息
道德声明
搜索
导航
#####
在A部分,178例首次接受EC治疗的患者被纳入。TP53mut 22例(12.4%),非TP53mut 156例(87.6%)。B部分纳入36例患者。TP53mut患者5例(13.9%),非TP53mut患者31例(86.1%)。除患者年龄外,甲、乙两部分患者的其他基线特征均无统计学差异。患者一般情况见表1。
表1 A组和B组患者特征
结果显示,TP53mut组高血压或糖尿病(p=0.011)、非子宫内膜样癌(p=0.006)和FIGO分期较高(p < 0.001)的比例较高。TP53mut患者的中性粒细胞、单核细胞和血小板计数明显高于非TP53mut患者(p=0.007、0.025,均< 0.001)。许多TP53mut患者LDL-C水平高于参考范围,差异有统计学意义(p=0.005)。TP53mut患者的HDL-C/LDL-C比例高于中位数0.5,差异有统计学意义(p=0.025)。CA125水平在TP53mut患者中高于非TP53mut患者(p=0.003)。此外,术前影像学显示更多的TP53mut患者有宫颈受累或下子宫受累(p < 0.001;表2)。
表2 A部分非TP53mut与TP53mut患者术前参数比较
术后病理特征包括腹水细胞学、淋巴血管间隙浸润(LVSI)、深肌层浸润(DMI)和淋巴结转移(LNM)。这些病理因素被分为是或否。术后病理特征单因素分析显示,TP53mut组腹水细胞学、DMI、LVSI、LNM阳性患者多于非TP53mut组(p=0.019, < 0.001, < 0.001, < 0.001;表3)。
表3 A部分非TP53mut与TP53mut患者术后病理特征比较
术前临床参数多因素分析结果显示,HDL-C/LDL-C、CA125水平、宫颈或下子宫受病是与TP53mut相关的独立影响因素(p=0.016、0.047,< 0.001;表4).根据logistic回归结果,建立TP53mut预后模态模型(nomogram prognosis model, TPMM): TPMM=-1.385 × HDL-C/LDL-C + 1.068 × CA125 + 1.89 × CI或LUI。根据预测模型构建nomogram,如图2所示。
表4术前参数预测TP53mut的多因素logistic分析
图2
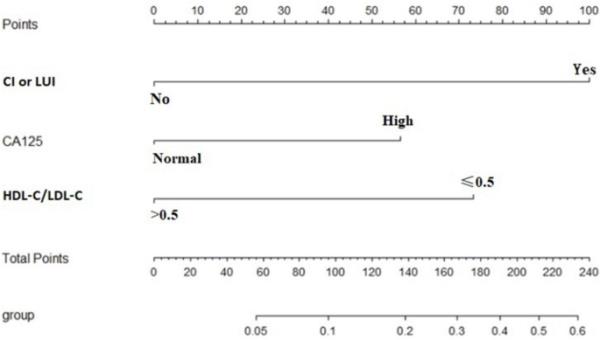
预测子宫内膜癌女性中TP53mut的概率的Nomogram。nomogram预后模型包括三个变量:HDL-C/LDL-C、CA125水平、CI或LUI
TPMM预测A部分和B部分TP53mut的auc分别为0.768 (95% CI, 0.642 ~ 0.893)和0.781 (95% CI, 0.581 ~ 0.980)。ROC曲线如图3所示。甲、乙两部分TPMM预测TP53mut疗效的诊断性能见表5。
图3
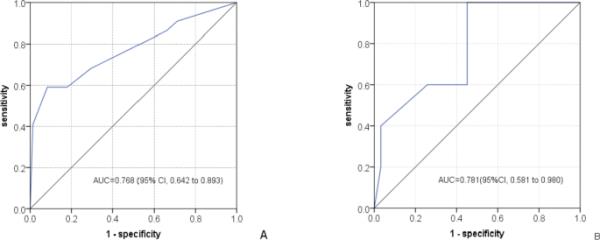
构建预测TP53mut模型的受试者工作特征(ROC)曲线。A部分的模型表示;B部分的模型表示
表5 TPMM预测甲、乙两部分TP53mut疗效的诊断性能
178例患者的中位随访时间为47个月(95% CI, 43-55个月)。复发18例(10.1%),死亡8例(4.5%)。TP53mut患者的PFS和OS较非TP53mut患者差(p < 0.001)。tpmm预测的TP53mut患者的PFS和OS也低于tpmm预测的非TP53mut患者(p < 0.001, 0.016;图4)。
图4
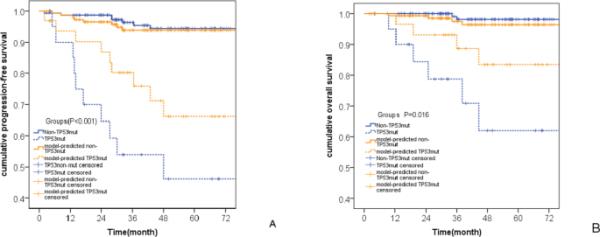
A部分TPMM预测结果与实际结果的比较A部分无进展生存期预测结果的比较;B总生存期预测的比较
鉴于分子分型与EC预后的显著相关性,EC分子分型在临床实践指南中被广泛推荐。由于四种分子亚型中TP53mut亚型的生存结局明显差于其他三种亚型,因此术前对TP53mut亚型患者的有效识别对于手术决策和治疗尤为重要。因此,本研究将TP53mut亚型与其他3个分子亚型进行二分类,筛选出与TP53mut相关的术前临床参数特征,构建并验证了由3个术前参数变量组成的nomogram预测模型TPMM。
在我们的研究中,TP53mut组患者的中性粒细胞和单核细胞计数明显高于非TP53mut组患者。事实上,近年来许多研究都支持全身性炎症反应在肿瘤的发生、发展和预后中的作用[15,16,17]。包括中性粒细胞、淋巴细胞和单核细胞在内的外周血细胞是肿瘤免疫的生物标志物,在全身炎症反应中起着至关重要的作用[18]。肿瘤组织释放的各种细胞因子可刺激中性粒细胞升高,从而为肿瘤的发生发展提供适宜的微环境。在癌患者中,中性粒细胞的功能更加多样化。它可以显示防御功能,并导致一些中性粒细胞的激活,促进肿瘤刺激因子。此外,中性粒细胞的增加还能抑制T淋巴细胞的活化,从而减弱对肿瘤生长的抑制作用[19]。大量研究也报道了单核细胞具有一些肿瘤功能,如分化为肿瘤相关巨噬细胞(tumor-associated macrophages, tam)、细胞因子转移、抑制T细胞、促进血管生成和细胞外基质重塑等[20]。tam可产生多种因子,如肿瘤生长因子、血管生成因子等,加速肿瘤的进展和侵袭[21]。单核细胞还可以通过限制活化的CD8 + T细胞向肿瘤微环境的浸润来促进免疫逃逸[22]。因此,单核细胞计数升高是肿瘤侵袭性的一个特征。此外,单核细胞是EC预后不良的独立预测因子,与肿瘤高级别、疾病晚期、淋巴结转移和腹水细胞学阳性相关[23,24]。也有报道称,单核细胞计数是预测肿瘤复发和进展的有用生物标志物[25]。显然,这些研究表明,中性粒细胞和单核细胞计数升高与预后较差有关。这与我们的研究结果一致,预后最差的TP53mut患者的中性粒细胞和单核细胞计数明显高于非TP53mut患者。这似乎解释了中性粒细胞和单核细胞计数升高与较差预后相关的机制,可能是由于与TP53突变有关。
P53参与调节多种代谢途径,包括脂质代谢[26],通过多种途径抑制脂质合成,促进脂质分解和脂肪酸氧化[27]。P53可以抑制甲羟戊酸途径,降低胆固醇合成。而P53发生突变时,会导致甲羟戊酸途径上调,增加胆固醇合成,促进肝癌、胰腺癌和乳腺癌的进展[28,29,30]。羟甲基戊二酰辅酶a还原酶是甲羟戊酸途径中的关键酶,其抑制剂为他汀类药物。大量临床研究支持他汀类药物和其他甲羟戊酸途径抑制剂的抗肿瘤作用[31,32],包括EC[33,34]。本研究脂质代谢分析显示,TP53mut患者LDL-C水平高于非TP53mut患者,且HDL-C/LDL-C比值更低。体内LDL-C是一种携带胆固醇进入外周组织细胞的脂蛋白颗粒,可被氧化成氧化低密度脂蛋白(OX-LDL)。当LDL-C,尤其是OX-LDL过量时,更多的胆固醇在动脉壁上积累,导致动脉粥样硬化。因此,LDL-C水平升高与动脉粥样硬化发生率增加有关,他汀类药物是动脉粥样硬化的有效药物,他汀类药物改善EC预后的机制似乎可以理解为降低LDL-C水平,从而减缓EC的进展。此外,在孟德尔随机研究中发现LDL-C与非子宫内膜EC之间存在关联。研究结果显示,LDL-C的降低与非子宫内膜样EC的风险呈负相关[35];换句话说,LDL-C的升高与非子宫内膜样癌的风险呈正相关。本研究结果还显示LDL-C升高与TP53突变有关,而TP53突变多为非子宫内膜样癌,因此我们的研究结果与该研究结果一致。
CA125作为临床常用的肿瘤生物标志物,其升高与EC预后不良相关。Toole等报道CA125可作为子宫内膜样癌淋巴结转移的术前危险分层因素,与淋巴结转移有显著相关性[36]。Li等也发现CA125≥35 U/ml的EC患者的淋巴结转移比例高于CA125 < 35 U/ml的EC患者[37]。我们的研究结果显示,CA125在TP53mut患者中较高,这可能是由于TP53mut患者的淋巴结转移率较高(21/22,95.5%)。
子宫内膜癌累及子宫颈或下子宫段与不良预后因素相关,如子宫肌层浸润、子宫浆液面累及、淋巴结转移和较高的组织学分级[38]。Cokmez等发现下子宫受累和淋巴血管腔浸润与淋巴结转移有显著相关性[39]。Kizer等人也发现,子宫下段受损伤与早期EC患者复发和死亡的高风险相关[40]。上述研究虽然通过术后病理检查确定下子宫段或宫颈受累,但通过术前影像学检查可以发现高比例的阳性患者。Yildirim等三维阴道超声对子宫深肌浸润、下子宫段和宫颈浸润的诊断准确率分别达到87.5%、80%和85%,MRI对下子宫段和宫颈浸润的诊断准确率更高[41]。本研究通过logistic回归分析显示,宫颈或下子宫受累是术前影像学检查与TP53mut相关的独立影响因素之一。
最后,我们构建了TP53mut预测模型(TPMM),在验证人群中具有较好的诊断准确性,生存分析表明该模型可以识别不同预后风险的患者。据我们所知,这是第一个基于术前临床参数构建EC TP53mut预测模型,并使用生存数据和验证样本对其进行验证的研究。该模型在临床实践中具有潜在的实用性,因为临床医生可以在术前时间点确认TP53突变信息,而不会对患者造成任何侵入性伤害。
然而,我们的研究也存在一些局限性。首先,我们的样本量有限,验证样本来自不同时期的单中心,实际上不是一个独立的验证集。其次,模型的稳健性可能受到潜在因素的影响,如长期使用他汀类降脂药物,长期使用阿司匹林等抗血小板药物。近期感染可影响中性粒细胞、单核细胞和淋巴细胞。宫颈受累或下子宫受累在模型中强烈依赖于放射科医生的经验,以准确解释图像。第三,我们在预测预后时没有考虑术后辅助治疗的因素,因此模型的预测结果与患者的真实预后存在差异。进一步开展多中心、更大样本量的研究,验证术前因素预测EC中TP53mut的有效性。
我们开发了一个高预测模型,TPMM,有三个术前无创参数来预测EC中的TP53mut亚型。该模型具有良好的诊断准确性,生存分析表明该模型可以识别不同预后风险的患者。这可以帮助妇科肿瘤学家在手术前计划患者的整体治疗。
下载原文档:https://link.springer.com/content/pdf/10.1186/s12885-023-11234-1.pdf








